Độ tan là gì? Công thức tính và các yếu tố ảnh hưởng đến độ tan của chất
Khái niệm độ tan là gì?
Độ tan được hiểu đơn giản là khả năng hòa tan của một chất ở trong nước để tạo ra dung dịch đồng nhất. Theo công thức tính độ tan, bạn có thể định nghĩa độ tan là số gam chất đó hòa tan trong 100g nước tạo thành dung dịch bão hòa. Chẳng hạn, ở nhiệt độ 25 độ C, độ tan của dung dịch natri clorua là 36g, độ tan của AgNO3 là 222g…
Có 2 yếu tố chính ảnh hưởng đến độ tan: Với chất rắn, độ tan phụ thuộc vào nhiệt độ, còn với chất khí, độ tan phụ thuộc vào cả nhiệt độ và áp suất.

Thế nào là chất tan và chất không tan
Để phân biệt được chất nào tan, chất nào không tan, bạn cần làm thí nghiệm để kiểm chứng, cụ thể:
Thí nghiệm về chất tan và chất không tan
Thông thường, người ta sẽ dựa vào độ tan của chất đó trong nước để xác định xem đó là chất tan hay chất không tan. Nếu 100g nước hòa tan >10g chất thì chất đó là chất tan. Nếu 100g nước chỉ hòa tan <1g chất đó, gọi là chất tan ít. Trong trường hợp 100g nước hòa tan < 0,01g chất sẽ được gọi là chất không tan.

NaCl tan được trong nước
Bạn có thể thí nghiệm canxi cacbonat và natri clorua vào 100g nước để kiểm tra sẽ thấy: CaCO3 không tan trong nước, NaCl tan được trong nước.
Như vậy, có thể thấy, trong thực tế, không phải mọi chất đều hòa tan được trong nước. Có chất tan nhiều, tan ít, hoặc không tan.
Tính tan của muối, axit, bazơ trong nước
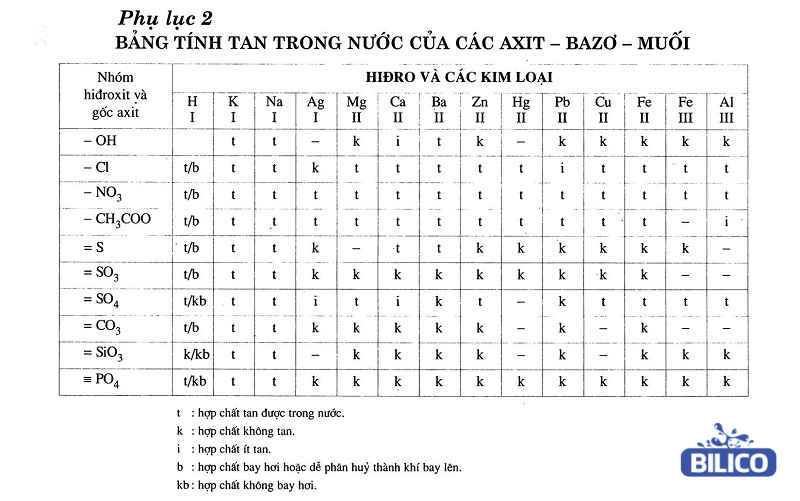
Bảng tính tan trong nước của các axit, bazơ, muối
Đối với axit: Trừ axit silixic, hầu hết các axit đều tan dễ dàng trong nước.
Đối với bazơ: Có một số bazơ ít tan trong nước như NaOH, Ca(OH)2, Ba(OH)2, còn lại các bazơ đều không tan trong nước.
Đối với muối: Tất cả các muối Na, -NO3, K, muối Na2CO3, muối K2CO3 đều tan trong nước. Phần lớn các muối clorua và sunfat cũng tan được trong nước, trừ BaSO4, AgCl, PbSO4. Muối cacbonat không tan trong nước.
Công thức tính độ tan CHUẨN của một chất trong nước
Để tính độ tan của một chất, ta dựa vào công thức tính sau:
S = (mct/mdm) x 100
Trong đó: mct là khối lượng chất tan, mdm là khối lượng dung môi, S là độ tan.
Với công thức tính này, ta có thể thấy độ tan càng nhỏ thì chất đó tan càng ít trong nước và ngược lại, nếu độ tan S lớn thì chất có tan nhiều trong nước.
Phân tích các yếu tố ảnh hưởng đến độ tan của một chất là gì?
Bên cạnh hai yếu tố chính là nhiệt độ và áp suất như đã nêu ở phần khái niệm độ tan, chúng tôi sẽ đi sâu vào 10 yếu tố ảnh hưởng đến độ tan của một chất, cụ thể:
#1. Yếu tố nhiệt độ
Bạn chỉ cần quan tâm đến hai chất khí và rắn. Đối với chất khí, nhiệt độ càng cao thì độ tan trong dung môi càng thấp và ngược lại. Đối với chất rắn thu nhiệt thì nhiệt độ càng cao, độ tan càng lớn. Trong khi đó, với chất rắn tỏa nhiệt, nhiệt độ càng cao thì độ tan càng thấp.
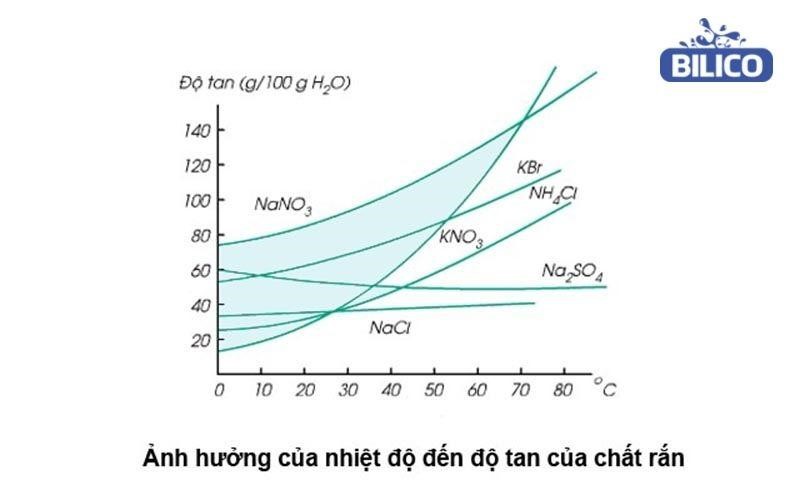
Nhiệt độ ảnh hưởng đến độ tan của chất rắn
#2. Yếu tố áp suất
Yếu tố áp suất chủ yếu áp dụng đối với chất khi. Nếu chất khí có độ tan thấp và áp suất không quá lớn thì lượng chất khí hòa tan trong chất lỏng tỉ lệ thuận với áp suất của nó trên bề mặt chất lỏng. Vì vậy, khi áp suất tăng, kéo theo độ tan tăng và ngược lại.
#3. Yếu tố hỗn hợp dung môi
Yếu tố dung môi cũng ảnh hưởng đến độ tan của một chất. Khi kết hợp hỗn hợp dung môi đồng tan với nước thì độ tan của các chất khó tan sẽ ngày càng cao hơn.
#4. Dựa vào độ phân cực của dung môi và chất tan
Bạn có thể phân chia thành các chất phân cực dễ tan trong dung môi như nước, muối, kiềm, axit vô cơ… Các chất ít phân cực dễ tan hơn như benzene, chloroform…
#5. Dựa vào hình dạng
Với chất rắn dạng không định hình thì có độ tan lớn hơn chất rắn dạng tinh thể. Tuy nhiên, chất rắn vô định thường có xu hướng chuyển về dạng tinh thể.

#6. Căn cứ vào các icon cùng tên
Khi người dùng tiến hành tăng nồng độ các icon cùng tên, chất tan có cân bằng điện ly dịch chuyển dần về phía dạng phân tử nên làm giảm độ tan. Vì vậy, trước khi thực hiện việc hòa tan một chất vào dung dịch (nước), bạn cần hòa tan chất ít tan, rồi hòa tan chất dễ tan.
#7. Dựa vào hiện tượng đa hình
Chất rắn có thể kết tinh thành nhiều dạng tinh thể khác nhau nên có độ tan và tính chất khác nhau. Với các chất có tinh thể kém bền cần ít năng lượng phá vỡ cấu trúc nên chất đó dễ tan trong nước. Tuy nhiên, phần lớn các chất này có xu hướng chuyển về dạng bền để làm giảm độ tan của chất rắn.
#8. Dựa vào hiện tượng hydrat hóa
Hiện tượng hydrat hóa cũng là một yếu tố ảnh hưởng đến độ tan của một chất. Trong quá trình kết tinh, chất rắn tồn tại ở dạng khan sẽ có độ tan lớn hơn chất rắn tồn tại ở dạng ngậm nước.
#9. Yếu tố chất điện ly
Chất điện li trong dung dịch có tác động làm giảm độ tan của chất tan. Vì vậy, bạn cần tiến hành pha loãng chất điện ly trước khi hòa vào dung dịch đảm bảo quá trình tan diễn ra ổn định.
#10. Căn cứ vào độ pH của dung dịch
Nếu axit hóa dung môi sẽ làm độ tan của các chất kiềm yếu sẽ tăng cao. Trong khi đó, nếu kiềm hóa dung môi thì axit yếu có độ tan tăng lên. Với các chất lưỡng tính, độ pH của dung dịch càng xa điểm đẳng điện, độ tan càng lớn và ngược lại.
Bảng tính tan trong nước của các axit, bazơ, muối
Dựa vào bảng tính tan hóa học của muối, axit, bazơ mà bạn có thể biết được chất nào tan, ít tan, tan nhiều hoặc không tan.
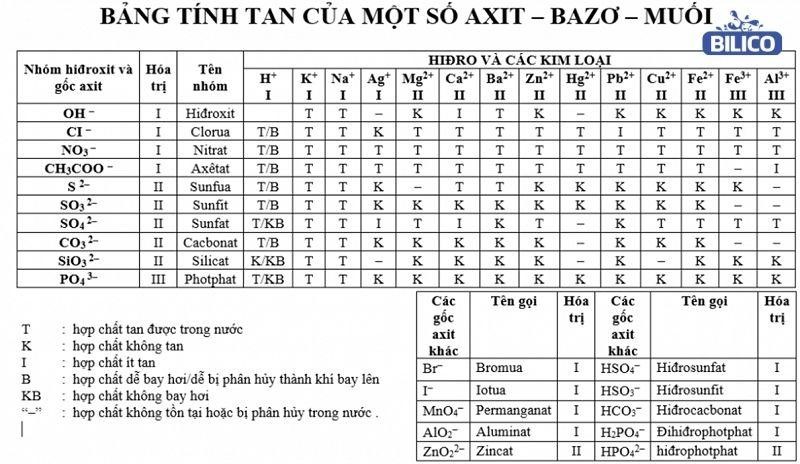
Trong đó, lưu ý: T là chất dễ tan, K là chất không tan, I là chất ít tan, “-” là chất không tồn tại.
Hướng dẫn cách đọc bảng tính tan nhanh nhất cho người dùng
Tùy từng chất cụ thể để bạn xác định được ion âm, ion dương và đối chiếu theo cột, hàng để biết trạng thái chất đó là tan hay không tan:
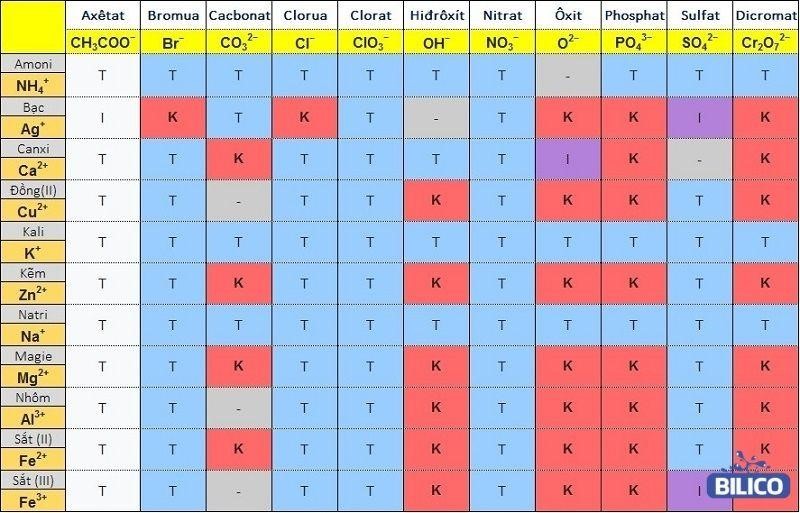
Bảng tính tan cập nhật CHUẨN NHẤT
Dựa vào bảng tính tan chi tiết
|
Hợp chất |
Tính chất | Ngoại trừ |
| Axit (xem tại cột ion H+ và anion gốc axit tương ứng) | Tan |
H2SiO3 |
| Bazo (xem tại hàng ion OH- và các cation tương ứng) | Không tan |
LiOH, NaOH, KOH, Ca(OH)2, Ba(OH)2, NH4OH. |
| – Muối liti
– Muối natri – Muối kali – Muối amoni |
Tan | |
| Muối bạc | Không tan (AgCl) |
AgNO3, CH3COOAg. |
| – Muối nitrat
– Muối axetat |
Tan | |
| – Muối clorua
– Muối bromua – Muối iotua |
Tan | AgCl: kết tủa trắng
AgBr: kết tủa vàng nhạt AgI: kết tủa vàng PbCl2, PbBr2, PbI2 |
| Muối sunfat | Tan | BaSO4, CaSO4, PbSO4: kết tủa trắng
Ag2SO4: ít tan |
| – Muối sunfit
– Muối cacbonnat |
Không tan | Trừ muối của kim loại kiềm và amoni NH4+ |
| Muối sunfua | Không tan | Trừ muối của kim loại kiềm, kiềm thổ và amoni NH4+ |
| Muối photphat | Không tan | Trừ muối với Na+, K+ và amoni NH4+ |
Dựa bài bài thơ tính tan của muối dễ nhớ
“Loại muối tan tất cả
là muối nitrat
Và muối a xê tát
Bất kể kim loại nào
Những muối hầu hết tan
Là clorua, sunfat
Trừ bạc chì clorua
Bari, chì sunfat
Những muối không hòa tan
Cacbonat, photphat
Sunfua và sunfit
Trừ kiềm, amoni”.
Bài viết trên đã giúp người đọc có thêm nhiều kiến thức hữu ích về độ tan là gì? Công thức tính độ tan, các yếu tố ảnh hưởng đến độ tan của một chất cũng như cách đọc bảng tính tan dễ thuộc. Qua đó, hy vọng bạn sẽ phân biệt được chất nào tan, chất nào không tan một cách nhanh nhất. Liên hệ ngay Bilico Miền Nam để được tư vấn trực tiếp hotline: 0912644646
Xem thêm: Chất khử là gì?